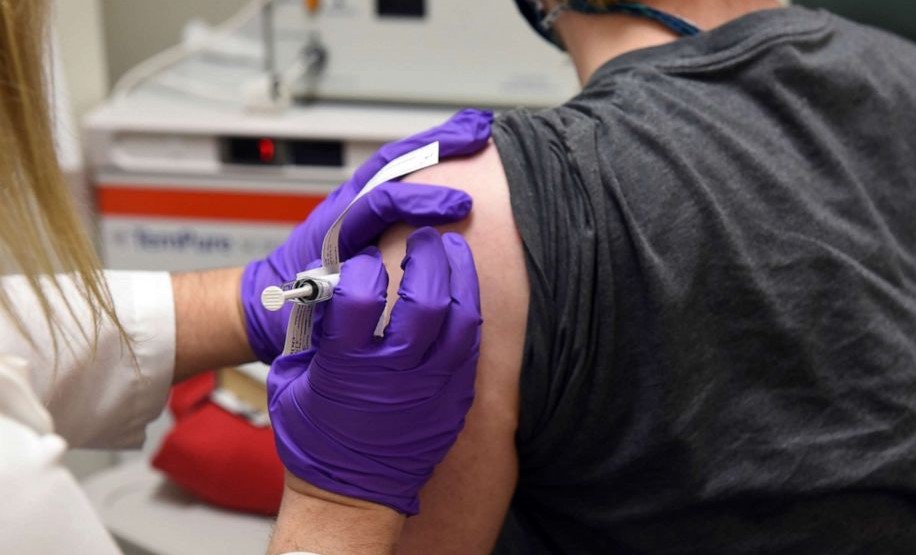
ファイザー社とパートナーのバイオエヌテックは現在臨床試験中(フェーズ3)のコロナウイルスワクチンの早期分析結果を公開、「90%以上の確率で患者を保護することが分かった」と発表した。
ファイザーのアルバート・ブーラCEO兼会長は声明の中で、「私たちは世界的な健康危機の突破口を提供する大きな一歩を踏み出した」と語った。
このワクチンは6か国、43,538人でテストされ、安全上の懸念は提起されていない。
ファイザー社は11月第3週に食品医薬品局(FDA)に緊急使用承認を申請する予定である。
ワクチンの専門家は、公開されたデータを有望と主張している。
FDAに助言する独立委員会メンバーのポール・オフィット博士(フィラデルフィア小児病院)は、「有望に見える」と述べた。
オックスフォード大学のジョン・ベル教授はBBCニュースの取材に対し、「自信を持って効果的と言える」と語った。
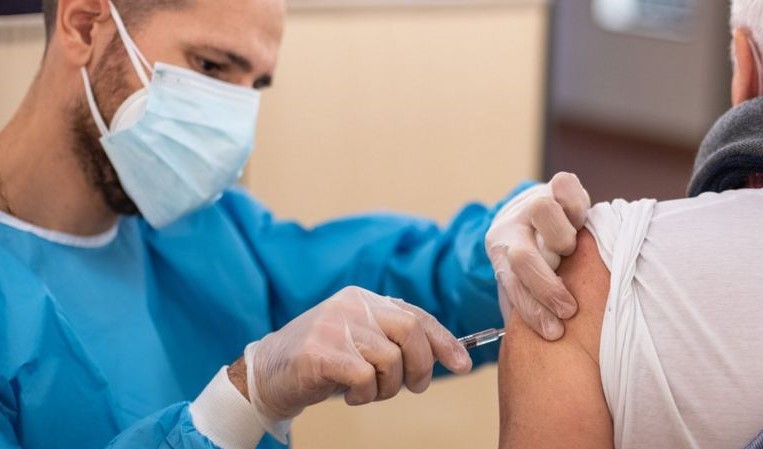
使用開始時期
ファイザー社は11月の第3週にFDA許可を申請する予定。公聴会と独立したワクチン諮問委員会からの報告後、緊急使用が許可される。認可までの期間は2~4週間。
FDAのガイダンスによると、企業は少なくとも2か月分の分析データを提供し、有効性を示さなければならないという。
オペレーション・ワープ・スピードのチーフアドバイザー、モンセフ・スラウイ博士はABCニュースの取材に対し、「全てが計画通りに進み、科学的または製造上の大きな遅れが発生しなければ、ほとんどのアメリカ人が2021年6月までに予防接種を受けることができるだろう」と述べた。
問題点
公開されたデータは暫定的なものであり、不明点も多い。
・ワクチンはウイルスの拡散を防止する?
・単に発症を抑えるだけ?
・免疫を保持できる期間は?
免疫保持期間の答えが出るのは、数カ月から数年かかるものと思われる。
また開発されたワクチンは、マイナス75℃前後の超低温貯蔵庫に保管する必要があり、保存や移送に大きな課題を抱えている。


ワクチン(Getty-Images)-1.jpg)
-1.jpg)
.jpg)
とイスラエルのネタニヤフ首相(Getty-Images/AFP通信).jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)

.jpg)

.jpg)
.jpg)
-1.jpg)

.jpg)
.jpg)
.jpg)

-2.jpg)
.jpg)
.jpg)